氯化铵溶液与熟石灰反应的化学方程式是什么?
如果是加热条件下或是浓溶液相互反应,NH3·H2O会分解放出NH32NH4Cl+Ca(OH)2==CaCl2+2NH3↑+2H2O如果是在冷稀溶液则得到NH3·H2O2NH4Cl+Ca(OH)2==CaCl2+2NH3·H2O碾磨是会放出氨气的,因为全是固体,得到NH3·H2O后它并不能稳定存在,会分解放出氨气2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑
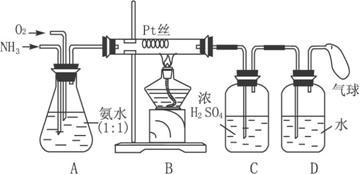
关于氯化铵和熟石灰加热反应的问题
ca(oh)2 =(1)氯化铵的相对分子质量为53.5g/mol,所以参加反应的氯化铵的物质的量是10.7/53.5=0.2mol。根据反映方程式可知,氯化铵的物质的量与生成的氨气的物质的量相同。所以氨气的体积v=0.2mol*22.4l/mol=4.48l.(2)第一问已知,氨气的物质的量为0.2mol,故氨水的物质的量浓度即为:氨气的物质的量除以氨水的体积。c=0.2mol/0.5l=0.4mol/l首先得到氯化铵的分子量是53.5,所以10.7g是0.2mol的氯化铵,那么与足量的熟石灰反映所有的氨气都会出来,也就是0.2mol的氨气,标准是22.4l/mol,所以第一问的答案是4.48l第二问就是用物质的量除以溶剂的体积就是8.96mol/l答:(1)5.97g(≈先写化学方程式吧:2NH4Cl接下来看题,要制取2500mL氨气,其中氮原子完全由氯化铵而来,二者的物质的量应该相等。n(NH3)=n(NH4Cl)。其中n(NH3)=2.5L22.4(L/mol)0.1116mol。所以氯化铵的物质的量也是这个数。通过这个求质量,又可以算出来NH4Cl摩尔质量等于53.5g/mol,所以m(NH4Cl)=53.5g/mol0.1116mol然后是第二问。要算物质的量浓度,首先肯定要算出溶质(氨)物质的量。n(NH3)=5L22.4(L/mol)0.2232mol。所以剩下的只要把这个数除以溶液体积就行了。【这里】我猜水溶液应该是100mL吧?100mol看着好奇怪的说。如果按照我猜测的做,物质的量浓度0.2232mol2.23mol/L。(1)2500ML约等于1.1MOL设需要NH4ClXMOL2NH4Cl+Ca(OH)2==CaCl2+2NH3+2H2O所以X=1.1MOL1.1MOL乘NH4Cl相对分子质量53.5约等于5.9克(2)第二问我也期待答案,这好像是高一教材后面总复习的题。
熟石灰与氯化铵溶液反应的方程式(要配平)及现象是什么?
2NH4Cl Ca(OH)2=CaCl2 2NH3(气) 2H2O有气体生成

会中毒吗我把氯化铵和熟石灰一起研磨?我把氯化铵和熟石灰一起研磨,
当然量不能很大而且对呼吸道也是有伤害的
氯化铵和熟石灰反应化学方程式
2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O2NH4CL+Ca(OH)2=加热=CaCl2+2H2O+2NH3气体上升符号2NH4Cl+Ca(OH)2=2NH3+CaCl2+2H2O.... ...................... 加热
2NH4Cl+Ca(OH)2====CaCl2+2NH3↑+2H2O2nh4cl+ca(oh)2=2nh3+cacl2+2h20条件:加热2NH4cl Ca(OH)2=CaCl2 2NH3↑ 2H2O 没有错

氯化铵溶液与熟石灰反应的化学方程式是什么?
如果是加热条件下或是浓溶液相互反应,NH3·H2O会分解放出NH3
2NH4Cl+Ca(OH)2==CaCl2+2NH3↑+2H2O
如果是在冷稀溶液则得到NH3·H2O
2NH4Cl+Ca(OH)2==CaCl2+2NH3·H2O
碾磨是会放出氨气的,因为全是固体,得到NH3·H2O后它并不能稳定存在,会分解放出氨气2nh4cl+ ca(oh)2===2nh3↑+ cacl2 + 2h2o
[或2nh4cl+ ca(oh)2===2nh3·h2o+ cacl2 ,nh3·h2o===nh3↑+h2o]





